Anvisa concede certificado de boas práticas de fabricação à Pfizer
Representantes do laboratório e da Agência de Vigilância Sanitária se reúnem amanhã em Brasília

Publicidade
A Agência Nacional de Vigilância Sanitária (Anvisa) e a farmacêutica Pfizer terão uma reunião nesta quarta-feira (30.dez) em Brasília para tentar avançar no debate sobre o registro da vacina contra covid-19 da farmacêutica no Brasil.
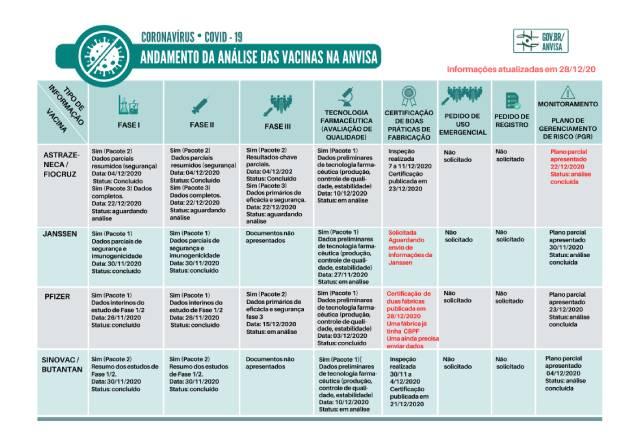
Ontem à noite, a Anvisa atualizou o andamento da análise das vacinas no país, certificando uma das fábricas da Pfizer/BioNtech que produzem o imunizante contra a covid-19. A outra fábrica ainda precisa enviar dados.
A certificação tem validade de dois anos e é um dos requisitos da análise do registro do imunizante. De acordo com a Anvisa, a etapa é "parte dos esforços contínuos da Agência para a disponibilização de vacinas com qualidade, segurança e eficácia para a população, no menor tempo possível".
Com o certificado, a Pfizer precisa apenas da aprovação do pedido de uso emergencial da vacina para receber chancela da Anvisa para iniciar a imunização da população. O mesmo certificado já foi concedido às fabricantes da AstraZeneca e da Sinovac.
Ao todo, participam quatro empresas nos processos de fabricação do insumo farmacêutico ativo biológico, bem como da formulação da vacina desenvolvida pela Pfizer/Biontech. Das quatro empresas, a Anvisa afirma ter informações suficientes de três delas quanto ao cumprimento das boas práticas de fabricação, restando pendente informações relativas a apenas uma.
A farmacêutica, no entanto, comunicou que optou pelo processo de "submissão contínua" da vacina à agência, por considerá-lo "mais célere" diante das regras apontadas no Guia de Submissão para Uso Emergencial, elaborado pela Anvisa.
No processo de submissão contínua, os dados técnicos da vacina são encaminhados à Anvisa à medida que são gerados. Assim sendo, as empresas interessadas no registro de vacinas contra Covid-19 não precisam ter em mãos todos os documentos reunidos para apresentá-los à agência.
Ontem à noite, a Anvisa atualizou o andamento da análise das vacinas no país, certificando uma das fábricas da Pfizer/BioNtech que produzem o imunizante contra a covid-19. A outra fábrica ainda precisa enviar dados.
A certificação tem validade de dois anos e é um dos requisitos da análise do registro do imunizante. De acordo com a Anvisa, a etapa é "parte dos esforços contínuos da Agência para a disponibilização de vacinas com qualidade, segurança e eficácia para a população, no menor tempo possível".
Com o certificado, a Pfizer precisa apenas da aprovação do pedido de uso emergencial da vacina para receber chancela da Anvisa para iniciar a imunização da população. O mesmo certificado já foi concedido às fabricantes da AstraZeneca e da Sinovac.
Ao todo, participam quatro empresas nos processos de fabricação do insumo farmacêutico ativo biológico, bem como da formulação da vacina desenvolvida pela Pfizer/Biontech. Das quatro empresas, a Anvisa afirma ter informações suficientes de três delas quanto ao cumprimento das boas práticas de fabricação, restando pendente informações relativas a apenas uma.

A farmacêutica, no entanto, comunicou que optou pelo processo de "submissão contínua" da vacina à agência, por considerá-lo "mais célere" diante das regras apontadas no Guia de Submissão para Uso Emergencial, elaborado pela Anvisa.
No processo de submissão contínua, os dados técnicos da vacina são encaminhados à Anvisa à medida que são gerados. Assim sendo, as empresas interessadas no registro de vacinas contra Covid-19 não precisam ter em mãos todos os documentos reunidos para apresentá-los à agência.
Publicidade









